МАРВЕЛОН таблетки №63

текст
- Безпосередньо в аптеці готівкою чи карткою
- Карткою онлайн
Детальніше
| Виробник | ОРГАНОСИН |
| Ознака виробника | Імпортний |
| Країна виробника | Індія |
| Бренд | МАРВЕЛОН |
| Первинна упаковка | блістер |
| Форма випуску | таблетки |
| Кількість в упаковці | 63 |
| Діюча речовина | Дезогестрел |
| Можна дорослим | Можна |
| Можна дітям | Ні |
| Можна вагітним | Ні |
| Можна годуючим | Ні |
| Можна алергікам | З обережністю |
| Можна діабетикам | З обережністю |
| Можна водіям | Можна |
| Спосіб застосування | внутрішньо |
| Взаємодія з їжею | Не має значення |
| Умови відпуску | За рецептом |
| Температура зберігання | не вище 30 С |
| Чутливість до світла | Ні |
Склад
діючі речовини: desogestrel, ethinylestradiol;
1 таблетка містить 0,150 мг дезогестрелу та 0,030 мг етинілестрадіолу;
допоміжні речовини: крохмаль картопляний; кремнію діоксид колоїдний безводний; альфа-токоферол; кислота стеаринова; повідон; лактоза, моногідрат.
Лікарська форма
Таблетки.
Основні фізико-хімічні властивості: круглі, двоопуклі таблетки білого кольору, з одного боку відтиснено слово ORGANON*, з іншого – напис TR/5.
Фармакотерапевтична група
Сечостатева система та статеві гормони. Статеві гормони і модулятори статевої системи. Гормональні контрацептиви для системного застосування. Естрогени і гестагени у фіксованих комбінаціях. Код АТХ G03A A09.
Фармакологічні властивості
Фармакодинаміка.
Марвелон® – це комбінований пероральний контрацептивний засіб, що містить 150 мкг дезогестрелу і 30 мкг етинілестрадіолу.
Етинілестрадіол – добре відомий синтетичний естроген.
Дезогестрел – це синтетичний прогестаген. Після перорального застосування чинить потужну дію, спрямовану на інгібування овуляції, виявляє потужну прогестагенну та антиестрогенну активність, не виявляє естрогенної активності, демонструє дуже слабку андрогенну/анаболічну активність.
Фармакокінетика дезогестрелу.
Всмоктування. Дезогестрел, прийнятий перорально, швидко та повністю всмоктується та перетворюється на етоногестрел. Пікова концентрація у сироватці на рівні майже 2 нг/мл досягається приблизно через 1,5 години після застосування разової дози. Біодоступність становить 62 – 81 %.
Розподіл. Етоногестрел зв’язується із сироватковим альбуміном та глобуліном, що зв’язує статеві гормони (ГЗСГ). Тільки 2 – 4 % загальної концентрації лікарського засобу в сироватці крові присутні у вигляді вільного стероїду, а 40 – 70 % специфічно зв’язані з ГЗСГ. Спричинене етинілестрадіолом збільшення ГЗСГ впливає на розподіл між білками сироватки крові, тим самим спричиняє збільшення ГЗСГ - зв’язаної фракції та зменшення зв’язаної з альбуміном. Очікуваний об’єм розподілу дезогестрелу – 1,5 л/кг.
Метаболізм. Етоногестрел повністю метаболізується відомими шляхами метаболізму стероїдів. Швидкість виведення метаболітів із сироватки крові становить приблизно 2 мл/хв/кг. Взаємодії з етинілестрадіолом, що приймається супутньо, не виявлено.
Виведення. Рівні етоногестрелу в сироватці крові зменшуються у два етапи. Кінцевий етап виведення характеризується часом напіввиведення приблизно 30 годин. Дезогестрел та його метаболіти виводяться разом із сечею і жовчю у співвідношенні приблизно 6:4.
Стан рівноваги. Рівень ГЗСГ, що зростає втричі під дією етинілестрадіолу, впливає на фармакокінетику етоногестрелу. Після щоденного застосування рівень речовини в сироватці крові зростає приблизно в 2 – 3 рази, досягаючи стабільної концентрації у другій половині циклу застосування лікарського засобу.
Фармакокінетика етинілестрадіолу.
Всмоктування. Після перорального застосування етинілестрадіол швидко і повністю всмоктується. Максимальна концентрація в сироватці крові на рівні приблизно 80 пг/мл досягається протягом 1 – 2 годин. Абсолютна біодоступність внаслідок пресистемної кон’югації і першого етапу метаболізму становить майже 60 %.
Розподіл. Етинілестрадіол характеризується сильним, але неспецифічним зв’язуванням із сироватковим альбуміном (приблизно 98,5 %) і спричиняє підвищення сироваткової концентрації ГЗСГ. Визначено, що очікуваний об’єм розподілу – 5 л/кг.
Метаболізм. Пресистемне кон’югування етинілестрадіолу відбувається як у слизовій тонкого кишечнику, так і в печінці. Етинілестрадіол спочатку метаболізується шляхом ароматичного гідроксилювання з утворенням великої кількості гідроксильованих і метильованих метаболітів, які присутні як вільні метаболіти і як сполуки з глюкуронідами та сульфатами. Швидкість метаболічного кліренсу – приблизно 5 мл/хв/кг.
Виведення. Рівень етинілестрадіолу в плазмі крові зменшується у два етапи, кінцевий етап виведення характеризується часом напіввиведення приблизно 24 години. У незміненому вигляді етинілестрадіол не виводиться; виведення метаболітів етинілестрадіолу відбувається разом із сечею і жовчю у співвідношенні 4:6. Період напіввиведення метаболітів – приблизно 1 доба.
Стан рівноваги. Рівноважні концентрації досягаються через 3 – 4 дні, коли рівень у сироватці на 30 – 40 % перевищує концентрацію після одноразової дози.
Показання
Пероральна контрацепція.
При розгляді питання про призначення лікарського засобу Марвелон® слід брати до уваги індивідуальні ризики у кожної окремої жінки, особливо ризик розвитку венозного тромбоемболізму (ВТЕ), а також порівняти ризик розвитку ВТЕ при застосуванні лікарського засобу Марвелон® та інших комбінованих гормональних контрацептивів (див. розділи «Протипоказання» та «Особливості застосування»).
Протипоказання
Комбіновані гормональні контрацептиви (КГК) не можна застосовувати за наявності будь-яких перелічених нижче станів. Якщо під час використання КГК вперше з'являються будь-які з перелічених нижче станів, застосування засобу слід негайно припинити.
Наявність або ризик розвитку венозного тромбоемболізму (ВТЕ).
- Венозний тромбоемболізм – наявність ВТЕ нині (проводиться лікування антикоагулянтами) або в анамнезі (наприклад тромбоз глибоких вен (ТГВ) або емболія легеневих судин (ЕЛС)).
- Відомі набуті або спадкові фактори ризику розвитку венозного тромбоемболізму, такі як резистентність до активованого протеїну С (включаючи V фактор Лейдена), дефіцит антитромбіну ІІІ, дефіцит протеїну С, дефіцит протеїну S.
- Обширне хірургічне втручання із тривалою іммобілізацією (див. розділ «Особливості застосування»).
- Високий ризик розвитку венозного тромбоемболізму внаслідок наявності множинних факторів ризику (див. розділ «Особливості застосування»).
Наявність або ризик розвитку артеріального тромбоемболізму (АТЕ)
- Артеріальний тромбоемболізм – наявність артеріального тромбоемболізму нині або в анамнезі (наприклад інфаркт міокарда) або продромального стану (наприклад стенокардія).
- Цереброваскулярне захворювання – наявність інсульту, в анамнезі – інсульт або продромальний стан (наприклад транзиторне ішемічне порушення мозкового кровообігу).
- Відома спадкова або набута схильність до розвитку артеріального тромбоемболізму, наприклад гіпергомоцистеїнемія і антитіла до антифософоліпідів (антитіла до антикардіоліпінів, вовчаковий антикоагулянт).
- Мігрень в анамнезі з фокальними неврологічними симптомами.
- Високий ризик розвитку артеріального тромбоемболізму внаслідок наявності множинних факторів ризику (див. розділ «Особливості застосування») або одного серйозного фактора ризику:
- цукровий діабет із судинними ускладненнями;
- тяжка форма артеріальної гіпертензії;
- тяжка форма дисліпопротеїнемії.
Панкреатит або раніше перенесений панкреатит, який асоціюється з високою гіпертригліцеридемією.
Наявність на даний час або в анамнезі тяжких захворювань печінки (доки показники функції печінки не повернуться до норми).
Наявність на даний час або в анамнезі пухлин печінки (доброякісних або злоякісних).
Встановлені або підозрювані естрогензалежні пухлини (див. розділ «Особливості застосування»).
Гіперплазія ендометрія.
Вагінальна кровотеча невстановленої етіології.
Встановлена або можлива вагітність.
Підвищена чутливість до будь-якого активного або допоміжного інгредієнта.
Марвелон® протипоказано застосовувати з комбінованою схемою лікування гепатиту С, яка містить омбітасвір/паритапревір/ритонавір з дасабувіром або без нього або препарати, що включають глекапревір/пібрентасвір (див. розділ «Особливості застосування»).
Взаємодія з іншими лікарськими засобами та інші види взаємодії
Застереження. Необхідно уважно прочитати інструкцію для медичного застосування супутнього лікарського засобу для встановлення можливих взаємодій.
Взаємодії між пероральними контрацептивами та іншими лікарськими засобами можуть призвести до проривної кровотечі та/або неефективності перорального контрацептиву. Про нижчезазначені взаємодії повідомляється в літературних джерелах.
Метаболізм у печінці. Можлива взаємодія з лікарськими або рослинними засобами, які індукують мікросомальні ферменти, зокрема ферменти Р450 (CYP), що призводить до підвищеного кліренсу статевих гормонів і може знизити ефективність комбінованих пероральних контрацептивів, в тому числі лікарського засобу Марвелон®. До таких лікарських засобів належать фенітоїн, фенобарбітал, примідон, босентан, карбамазепін, рифампіцин та, можливо, окскарбазепін, топірамат, фельбамат, гризеофульвін, деякі інгібітори протеази ВІЛ (наприклад ритонавір) і ненуклеозидні інгібітори зворотної транскриптази (наприклад ефавіренз) та лікарські засоби, що містять рослинний компонент звіробій.
Індукція ферментів може спостерігатися через кілька днів лікування. Максимальна індукція ферментів зазвичай спостерігається протягом декількох тижнів. Після припинення застосування лікарського засобу індукція ферментів може тривати протягом приблизно 28 днів.
При супутньому застосуванні з гормональними контрацептивами багато інгібіторів протеази ВІЛ (наприклад нелфінавір) і ненуклеозидних інгібіторів зворотної транскриптази (наприклад невірапін) та/або лікарські засоби проти вірусу гепатиту С (ВГС) (наприклад боцепревір, телапревір) можуть збільшувати або зменшувати плазмові концентрації прогестину, в тому числі етоногестрелу, активного метаболіту дезогестрелу, або естрогенів. Чистий ефект цих змін в деяких випадках може бути клінічно значущим.
Жінкам, які приймають будь-який із цих лікарських або рослинних засобів, що індукують ферменти печінки, слід мати на увазі, що ефективність лікарського засобу Марвелону® може бути зменшена. Під час прийому засобів, що стимулюють мікросомальні ферменти, слід застосовувати бар’єрний метод контрацепції як доповнення до лікарського засобу Марвелон® протягом усього терміну застосування лікарського засобу, що стимулює мікросомальні ферменти, та протягом 28 днів після припинення застосування такого лікарського засобу.
Якщо період прийому супутнього лікарського засобу поширюється за межі прийому активних таблеток з упаковки КПК, наступну упаковку слід починати без звичайної перерви у застосуванні таблеток. У разі тривалого лікування ферментостимулюючими засобами слід розглянути альтернативний метод контрацепції, на який не впливають лікарські засоби, що стимулюють мікросомальні ферменти.
Одночасне застосування з потужними (наприклад кетоконазол, ітраконазол, кларитроміцин) або помірними (наприклад флуконазол, дилтіазем, еритроміцин) інгібіторами CYP3A4 може призвести до підвищення сироваткових концентрацій естрогенів або прогестинів, в тому числі етоногестрелу, активного метаболіту дезогестрелу.
Пероральні контрацептиви можуть впливати на метаболізм інших лікарських засобів. Відповідно, у плазмі крові та в тканинах концентрації таких лікарських засобів можуть підвищуватися (наприклад циклоспорину) чи знижуватися (наприклад ламотриджину).
В ході клінічних досліджень комбінованої схеми лікування гепатиту С, яка містить омбітасвір/паритапревір/ритонавір з дасабувіром або без нього, підвищення рівнів АЛТ більше ніж в 5 разів вище верхньої межі норми (ВМН) достовірно частіше зустрічалося у жінок, що застосовували засоби, які містять етинілестрадіол (КГК). Також у жінок, що застосовували етинілестрадіол (КГК), спостерігалось підвищення рівня АЛТ при одночасному застосуванні препаратів глекапревіру/пібрентасвіру. Застосування Марвелону® слід припинити до початку комбінованого лікування гепатиту С, яке містить омбітасвір/паритапревір/ритонавір з дасабувіром або без нього або препарати глекапревіру/пібрентасвіру (див. розділи «Протипоказання» та «Особливості застосування»). Поновлювати застосування Марвелону® слід приблизно через 2 тижні після завершення комбінованого лікування.
Лабораторні аналізи. Використання контрацептивних стероїдів може вплинути на результати певних лабораторних тестів, включаючи біохімічні показники функцій печінки, нирок, щитовидної залози, надниркових залоз, рівень білків (переносників) в сироватці крові, наприклад глобуліну, що зв’язує кортикостероїди та/або ліпідну/ліпопротеїнову фракції, показники вуглеводного обміну, коагуляції та фібринолізу. Зміни зазвичай залишаються в межах норми.
Особливості щодо застосування
За наявності будь-якого із зазначених нижче станів/факторів ризику призначення терапії лікарським засобом Марвелон® слід обговорити з жінкою. У разі загострення, посилення або першої появи будь-якого із цих станів жінка має звернутись до лікаря. Лікар повинен визначити, чи потрібно припинити застосування КГК.
Порушення кровообігу.
Ризик розвитку венозного тромбоемболізму (ВТЕ)
Застосування будь-якого КГК підвищує ризик розвитку венозного тромбоемболізму (в порівнянні з ризиком, коли КГК не застосовуються). Лікарські засоби, що містять левоногестрел, норгестимат або норетистерон, асоційовані з мінімальним ризиком розвитку ВТЕ. Інші лікарські засоби, такі як Марвелон®, можуть підвищувати ризик в 2 рази. Рішення про застосування будь-якого контрацептиву, який не є лікарським засобом з мінімальним ризиком розвитку ВТЕ, можна приймати тільки після обговорення з жінкою ризиків розвитку ВТЕ при застосуванні лікарського засобу Марвелон®, впливу її індивідуальних факторів на цей ризик, а також того, що ризик розвитку ВТЕ є максимальним упродовж першого року застосування лікарського засобу. Також ризик підвищується при відновленні застосування КГК, якщо перерва становила 4 тижні або більше.
Серед жінок, які не застосовують КГК і не вагітні, у двох із 10 000 розвиватиметься ВТЕ упродовж першого року. Проте у кожної окремої жінки ризик може бути набагато вищий, залежно від основних чинників ризику.
Встановлено1, що з 10 000 жінок, які застосовують КГК, що містить дезогестрел, у 9 – 12 жінок через 1 рік розвиватиметься ВТЕ; для порівняння при застосуванні КГК, що містять левоногестрел, ВТЕ виникатиме у 62 жінок.
В обох випадках кількість випадків ВТЕ в рік менша, ніж очікувана кількість при вагітності і в післяпологовий період.
ВТЕ може бути летальним в 1 – 2 % випадків.
1 Частота встановлена за даними епідеміологічного дослідження з використанням відносних ризиків для різних лікарських засобів в порівнянні з КГК, що містять левоногестрел.
2 Середній діапазон від 5 до 7 на 10 000 жінок-років встановлено за відносним ризиком при застосуванні КГК, що містять левоногестрел, в порівнянні з незастосуванням засобу - від 2,3 до 3,6.
Кількість випадків ВТЕ на 10000 жінок за 1 рік
- Дуже рідко повідомлялося про тромбоз, який виникав в інших кровоносних судинах, наприклад печінкових, мезентеріальних, ниркових, мозкових або ретинальних венах і артеріях, у жінок, що застосовували КГК.
Фактори ризику розвитку ВТЕ
- При застосуванні КГК ризик тромбоемболічних венозних ускладнень може істотно підвищуватися у жінок з додатковими факторами ризику, особливо за наявності множинних ризиків (див. таблицю 1).
- Лікарський засіб Марвелон® протипоказаний жінкам з множинними факторами ризику, які призводять до високого ризику розвитку венозного тромбозу (див. розділ «Протипоказання»). Якщо у жінки більше ніж один фактор ризику, можливо, що міра підвищення ризику буде вища, ніж сума індивідуальних факторів. У такому разі слід проаналізувати загальний ризик розвитку ВТЕ у жінки. Якщо співвідношення переваг і ризиків є несприятливими, не слід призначати КГК (див. розділ «Протипоказання»).
Таблиця 1
Фактори ризику ВТЕ
|
Фактор ризику |
Коментар |
|
Ожиріння (індекс маси тіла (ІМТ) більше 30 кг/м2). |
Ризик істотно підвищується при збільшенні ІМТ. Особливо важливо враховувати наявність інших факторів ризику. |
|
Тривала іммобілізація, обширне хірургічне втручання, будь-яке хірургічне втручання на ногах або органах таза, нейрохірургія, велика травма. Примітка. Тимчасова іммобілізація, включаючи авіаперельоти тривалістю більше 4 годин, також може бути фактором ризику розвитку ВТЕ, особливо у жінок з іншими факторами ризику. |
Рекомендовано припинити використання пластиря/таблеток/кільця (у разі елективної хірургії – як мінімум за 4 тижні до її проведення) і не поновлювати раніше ніж через 2 тижні після повного відновлення рухливості. Для запобігання вагітності слід використовувати інші засоби контрацепції. Слід розглянути питання про антитромботичну терапію, якщо застосування лікарського засобу Марвелон® не було припинено заздалегідь. |
|
Позитивний сімейний анамнез (венозний тромбоемболізм у брата/сестри або батьків, особливо у відносно ранньому віці, тобто до 50 років). |
Якщо підозрюється наявність вродженої схильності, перед ухваленням рішення про застосування будь-якого КГК жінку слід направити на консультацію до фахівця. |
|
Інші медичні стани, які супроводжуються ВТЕ. |
Рак, системний червоний вовчак, гемолітичний уремічний синдром, хронічне запальне захворювання кишечника (хвороба Крона або виразковий коліт) і серпоподібноклітинна анемія. |
|
Вік |
Особливо після 35 років. |
- Немає єдиної думки про можливу роль варикозу вен і поверхневого тромбофлебіту у виникненні або прогресуванні венозного тромбозу.
- Слід брати до уваги підвищений ризик тромбоемболізму в період вагітності, особливо протягом 6 тижнів після пологів (див. розділ «Застосування у період вагітності або годування груддю»).
Симптоми ВТЕ (тромбоз глибоких вен і емболія легеневих судин)
У разі виникнення симптомів жінка повинна негайно звернутися по медичну допомогу, повідомивши лікаря про те, що вона приймає КГК.
Симптоми тромбозу глибоких вен (ТГВ) можуть включати:
- односторонній набряк ноги та/або стопи або набряк по ходу вени ноги;
- біль або хворобливість в нозі, яка відчувається тільки при стоянні або ходьбі;
- тепліша на дотик уражена кінцівка; почервоніння або зміна кольору шкіри ноги.
Симптоми емболії легеневих судин можуть включати:
- раптова задишка або швидке дихання;
- раптовий кашель, який може супроводжуватися кровохарканням;
- гострий біль в грудній клітці;
- сильне запаморочення;
- швидке або нерегулярне серцебиття.
Деякі з цих симптомів (наприклад задишка, кашель) є неспецифічними і можуть бути помилково прийняті за такі, що часто виникають або є менш тяжкими (наприклад при інфекції респіраторного тракту).
Інші ознаки оклюзії судин можуть включати раптовий біль, набряклість і злегка синюшний відтінок шкіри кінцівки.
Якщо відбувається оклюзія судин ока, симптоми можуть варіювати від болючої нечіткості зору до втрати зору. Іноді втрата зору може виникати практично негайно.
Ризик артеріального тромбоемболізму (АТЕ)
- Епідеміологічні дослідження встановили зв’язок між застосуванням КГК і підвищеним ризиком розвитку артеріального тромбоемболізму (інфаркт міокарда) або порушень мозкового кровообігу (таких як транзиторне порушення мозкового кровообігу, інсульт). Артеріальні тромбоемболічні реакції можуть бути летальними.
Фактори ризику розвитку АТЕ
- Ризик розвитку артеріальних тромбоемболічних ускладнень або порушення мозкового кровообігу при застосуванні КГК підвищується у жінок з факторами ризику (див. таблицю 2). Лікарський засіб Марвелон® протипоказаний жінкам з одним серйозним або з множинними чинниками ризику розвитку АТЕ, які призводять до високого ризику артеріального тромбозу (див. розділ «Протипоказання»). Якщо у жінки більше ніж один фактор ризику, можливо, що міра підвищення ризику буде більшою за суму індивідуальних факторів. У такому разі слід проаналізувати загальний ризик для жінки. Якщо вважається, що співвідношення переваг і ризиків є несприятливим, КГК призначати не слід (див. розділ «Протипоказання»).
Таблиця 2
Фактори ризику розвитку АТЕ
|
Фактор ризику |
Коментар |
|
Вік |
Особливо після 35 років. |
|
Паління |
Під час застосування КГК жінці рекомендується припинити паління. Жінкам віком понад 35 років, які продовжують палити, наполегливо рекомендується застосовувати інший спосіб контрацепції. |
|
Артеріальна гіпертензія |
|
|
Ожиріння (індекс маси тіла більше 30 кг/м2) |
Ризик істотно підвищується при збільшенні ІМТ. Особливо важливо враховувати наявність інших факторів ризику. |
|
Позитивний сімейний анамнез (артеріальний тромбоемболізм у брата/сестри або батьків, особливо у відносно ранньому віці, тобто до 50 років) |
Якщо підозрюється наявність вродженої схильності, перед ухваленням рішення про застосування КГК жінку слід направити на консультацію до фахівця. |
|
Мігрень |
Підвищення частоти або тяжкості мігрені під час застосування КГК (що може бути продромальним симптомом при порушенні мозкового кровообігу) може бути причиною для негайної відміни лікарського засобу. |
|
Інші медичні стани, які супроводжуються побічними реакціями з боку судин |
Цукровий діабет, гіпергомоцистеїнемія, захворювання клапанів серця, фібриляція передсердя, дисліпопротеїнемія і системний червоний вовчак. |
Симптоми АТЕ
У разі виникнення симптомів жінка повинна негайно звернутися за медичною допомогою, повідомивши лікаря про те, що вона приймає КГК.
Симптоми порушення мозкового кровообігу можуть включати:
- раптове оніміння або слабкість в ділянці обличчя, в руці або нозі, особливо з одного боку тіла;
- раптове порушення ходи, запаморочення, порушення рівноваги або координації;
- раптова сплутаність свідомості, порушення мовлення або розуміння;
- раптове порушення зору в одному оці або в обох;
- раптовий інтенсивний або тривалий головний біль, що виник без певної причини;
- втрата свідомості або непритомність з/без судом.
Тимчасові симптоми вказують на транзиторну ішемічну атаку (ТІА).
Симптоми інфаркту міокарда можуть включати:
- біль, дискомфорт, почуття тиску, тяжкості, стискування або переповненості в грудній клітці, руці або нижче груднини;
- дискомфорт з іррадіацією в спину, щелепу, горло, руку, шлунок;
- відчуття переповненості шлунка, диспепсія або запор;
- пітливість, нудота, блювання або запаморочення;
- надзвичайна слабкість, тривожність або задишка;
- швидке і нерегулярне серцебиття.
Пухлини
Певні дослідження показали підвищений ризик раку шийки матки у жінок, які протягом тривалого часу застосовують КПК, проте, як і раніше, існує невизначеність щодо ступеня обумовлення захворювання супутніми ефектами, наприклад відмінностями у сексуальній поведінці або іншими факторами, як, наприклад інфікування вірусом папіломи людини (ВПЛ).
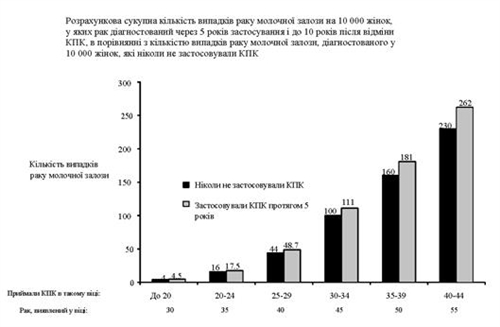
- Метааналіз 54 епідеміологічних досліджень показав, що існує незначне збільшення відносного ризику (ВР = 1,24) виявлення раку молочної залози у жінок, які на даний момент застосовують комбіновані пероральні контрацептиви (КПК). Випадки раку молочної залози, що діагностують у жінок, які приймають КПК на даний момент або застосовували КПК в останні десять років, більш імовірніше локалізуватимуться в молочній залозі, ніж діагностовані випадки раку у жінок, які ніколи не приймали КПК.
- Рак молочної залози рідко виникає у жінок до 40 років, незалежно від того, чи застосовують вони КПК. Оскільки цей фоновий ризик зростає з віком, додаткова кількість випадків раку молочної залози у тих жінок, що застосовують КПК тепер або застосовували їх раніше, є малою у порівнянні із загальним ризиком розвитку раку молочної залози (див. графік).
- Найважливішим фактором ризику раку молочної залози у тих, хто застосовує КПК, є вік, в якому жінка припиняє приймати КПК; чим старша жінка при припиненні застосування, тим вища вірогідність діагностування раку молочної залози. Тривалість застосування менш важлива, і підвищений ризик поступово зникає протягом 10 років після припинення застосування КПК настільки, що через 10 років ризик вже не перевищує звичайний.
- Можливе підвищення ризику раку молочної залози слід обговорити з жінкою і зважити переваги застосування КПК з урахуванням даних про те, що КПК забезпечують значний захист від ризику розвитку деяких інших видів раку (рак яєчників та ендометрію), див. нижче наведений графік.
- В іншому епідеміологічному дослідженні за участю 1,8 млн жінок з Данії, за якими спостерігали в середньому 10,9 року, повідомлялося, що ВР виявлення раку молочної залози у тих, хто застосовує КПК, збільшується при тривалому їх застосуванні у порівнянні з жінками, які ніколи не застосовували КПК (загальний ВР = 1,19; показник ВР знаходився в діапазоні від 1,17 при застосуванні КПК від 1 до 5 років та до 1,46 при застосуванні КПК понад 10 років). Відома абсолютна різниця у ВР (кількість випадків виникнення раку молочної залози у жінок, які ніколи не застосовували КПК, порівняно з тими, хто застосовує КПК наразі або нещодавно закінчили прийом) була невеликою: 13 на 100 000 пацієнто-років.
- Епідеміологічні дослідження не надають доказів причинної обумовленості таких даних. Модель підвищеного ризику, яка спостерігається, може бути пов’язана з більш ранньою діагностикою раку молочної залози у жінок, що застосовували КПК, біологічними ефектами КПК або комбінацією обох чинників.
- У жінок, які застосовували КГК, у рідкісних випадках повідомлялося про доброякісні і, набагато рідше, про злоякісні пухлини печінки. В окремих випадках такі пухлини призводили до небезпечних для життя внутрішньочеревних кровотеч. Таким чином, пухлини печінки слід враховувати при диференціальній діагностиці, якщо у жінок, які застосовують КГК, виникає біль у верхній частині живота, спостерігаються збільшення печінки або ознаки внутрішньочеревного крововиливу.
Гепатит С
- В ході клінічних досліджень комбінованої схеми лікування гепатиту С, яка містить омбітасвір/паритапревір/ритонавір з дасабувіром або без нього, підвищення рівня АЛТ більше ніж в 5 разів вище верхньої межі норми (ВМН) достовірно частіше зустрічалося у жінок, що застосовували лікарські засоби, які містять етинілестрадіол (КГК). Також у жінок, що застосовували етинілестрадіол (КГК), спостерігалось підвищення рівня АЛТ при одночасному застосуванні препаратів глекапревіру/пібрентасвіру. Застосування Марвелону® слід припинити до початку комбінованого лікування гепатиту С, яке містить омбітасвір/паритапревір/ритонавір з дасабувіром або без нього або глекапревір/пібрентасвір (див. розділи «Протипоказання» та «Взаємодія з іншими лікарськими засобами та інші види взаємодій»). Поновлювати застосування лікарського засобу Марвелон® слід приблизно через 2 тижні після завершення комбінованого лікування.
Інші стани.
- При застосуванні КПК у жінок із гіпертригліцеридемією або з її наявністю в сімейному анамнезі можливий підвищений ризик розвитку панкреатиту.
- Екзогенні естрогени можуть викликати або посилити симптоми спадкового та набутого ангіоневротичного набряку.
- Хоча повідомлялося про незначне підвищення артеріального тиску у багатьох жінок, які приймають КПК, клінічно значущі підвищення зустрічаються рідко. Взаємозв’язок між прийомом КПК і клінічною гіпертензією не встановлено. Однак, якщо тривала клінічно значуща артеріальна гіпертензія розвивається на фоні застосування КПК, лікар має заборонити застосування КПК та лікувати артеріальну гіпертензію. Застосування КПК можна відновити у разі нормалізації артеріального тиску за допомогою антигіпертензивної терапії.
- Повідомлялося про виникнення або погіршення таких станів при вагітності і при застосуванні КПК: жовтяниця та/або свербіж, пов’язані з холестазом; утворення каменів у жовчному міхурі; порфірія; системний червоний вовчак; гемолітико-уремічний синдром; хорея Сиденгама; герпес вагітних; втрата слуху, пов’язана з отосклерозом.
- Гострі або хронічні порушення функції печінки вимагають негайного припинення використання КПК доти, доки печінкові проби не повернуться до прийнятних показників. Рецидиви жовтяниці та/або свербіжу, пов’язані з холестазом, які виникали раніше під час вагітності або використання статевих стероїдів, також вимагають припинення прийому КПК.
- Хоча КПК можуть впливати на периферійну резистентність до інсуліну та порушення толерантності до глюкози, немає необхідності змінювати схеми лікування хворих на цукровий діабет, які приймають КПК. Однак, за жінками, хворими на цукровий діабет, має бути ретельний нагляд під час застосування КПК.
- Хлоазма може періодично виникати, особливо у жінок з наявністю в анамнезі хлоазми вагітних. Жінкам зі схильністю до хлоазми рекомендується під час застосування даного лікарського засобу уникати перебування на сонці або під дією ультрафіолетового випромінювання.
- Хвороба Крона і неспецифічний виразковій коліт пов’язані з прийомом КПК.
- Лікарський засіб Марвелон® містить лактозу (<80 мг у 1 таблетці). При рідкій спадковій непереносимості галактози, лактазній недостатності Лаппа або мальабсорбції глюкози/галактози не рекомендовано застосовувати даний лікарський засіб.
Медичне обстеження
Перед початком або відновленням застосування лікарського засобу Марвелон® лікар має уважно ознайомитися з особистим та сімейним анамнезом жінки і виключити вагітність. Враховуючи протипоказання (див. розділ «Протипоказання») і застереження (див. розділ «Особливості застосування») щодо застосування цього лікарського засобу, проводять повний медичний огляд та вимірюють артеріальний тиск. Жінці слід надати інформацію щодо венозного та артеріального тромбозу, включаючи дані про ризики при застосуванні лікарського засобу Марвелон® у порівнянні із іншими КГК, щодо симптомів ВТЕ та АТЕ, відомих факторів ризику та щодо дій при підозрі на тромбоз. Також, жінці слід пояснити, що вона повинна ретельно перечитати інструкцію для медичного застосування лікарського засобу і дотримуватися вказаних у ній рекомендацій. Частоту і характер обстеження визначає лікар, враховуючи офіційні практичні рекомендації, індивідуально для кожної окремої жінки.
Жінку слід попередити, що гормональні контрацептиви не захищають від ВІЛ-інфекції (СНІДу) та інших захворювань, які передаються статевим шляхом. Якщо існує такий ризик зараження (у тому числі і під час вагітності або після пологів), рекомендується адекватне використання презерватива з іншими методами контрацепції.
Зменшення ефективності.
Ефективність застосування лікарського засобу Марвелон® може знижуватись, наприклад у разі пропуску застосування таблеток, виникнення шлунково-кишкових розладів (див. розділ «Спосіб застосування та дози») або при одночасному застосуванні деяких лікарських засобів, які знижують концентрацію в плазмі крові етоногестрелу, активного метаболіту дезогестрелу (див. розділ «Взаємодія з іншими лікарськими засобами та інші види взаємодій»).
Погіршення контролю менструального циклу.
Під час застосування КГК можливі нерегулярні (незначні або рясні) кровотечі, особливо протягом перших місяців застосування. Тому оцінка будь-яких нерегулярних кровотеч може бути коректною лише після адаптаційного періоду, який становить приблизно три цикли.
Якщо нерегулярні кровотечі зберігаються або виникають після попередніх регулярних циклів, слід розглянути негормональні причини і призначити адекватні діагностичні заходи, включаючи кюретаж, для виключення вагітності або злоякісної пухлини.
У деяких жінок під час інтервалу без таблеток кровотеча відміни може не спостерігатися. Якщо КГК застосовували відповідно до рекомендацій, наведених у розділі «Спосіб застосування та дози», то можливість вагітності невелика. Проте якщо були порушення цих рекомендацій до першої відсутності кровотечі відміни в період без таблеток або якщо кровотечі відміни відсутні двічі підряд, перед тим як продовжити приймати КГК, потрібно виключити можливу вагітність.
Застосування у період вагітності або годування груддю.
Вагітність
Вагітність є протипоказанням для застосування лікарського засобу Марвелон®. Якщо жінка завагітніла під час застосування лікарського засобу Марвелон®, подальше застосування слід припинити. Однак, розширені епідеміологічні дослідження не виявили ні підвищення ризику патологій у дітей, матері яких приймали КПК до вагітності, ні тератогенних ефектів КПК, які ненавмисно застосовували на початку вагітності.
Слід пам’ятати про підвищений ризик ВТЕ в післяпологовий період при поновленні застосування лікарського засобу Марвелон® (див. розділи «Спосіб застосування та дози» та «Особливості застосування»).
Годування груддю
КПК можуть впливати на годування груддю, оскільки вони можуть зменшити кількість і змінити склад грудного молока. Таким чином, застосування КПК зазвичай не рекомендується до повного закінчення періоду годування груддю. З грудним молоком можуть виділятися малі кількості контрацептивних стероїдів та/або їх метаболітів, але немає жодних доказів, що це негативно впливає на здоров’я немов
ВІДГУКИ МАРВЕЛОН таблетки №63
Відгуків ще немає